Der pH-Wert ist ein Maß für die Konzentration einer Säure – also wie sauer eine wässrige Lösung reagiert. So weit so gut. Mit der genauen Definition, dass es sich hierbei um den negativen dekadischen Logarithmus der Wasserstoffionenkonzentration handelt, kann man in der kosmetischen Praxis allerdings herzlich wenig anfangen. Anschaulicher ist da schon die relative Säurekonzentration wie sie im folgenden vereinfachten Diagramm dargestellt und nachfolgend an Beispielen erläutert wird:
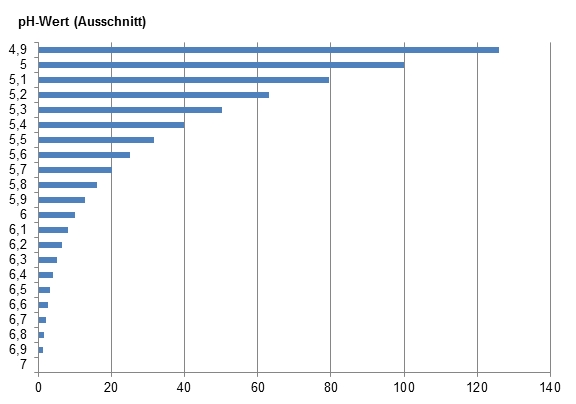
Relative Säurekonzentration (vereinfacht)
- Eine wässrige Lösung – wie etwa die Wasserphase einer Creme – ist mit pH-Wert 7 neutral, d. h. weder sauer (pH kleiner als 7) noch basisch (pH größer als 7).
- Wässrige Lösungen mit pH-Wert 5 sind 10-mal saurer im Vergleich zu pH 6 und etwa 100-mal saurer im Vergleich zu pH 6,9. Zwischen den vollen pH-Werten liegt also immer ein Faktor von 10 hinsichtlich der Säurekonzentration.
- Wässrige Lösungen mit pH-Wert 6 gelten als schwach sauer.
- Magensäure hat wie verdünnte Salzsäure einen pH-Wert von etwa 1. Das entspricht der 100.000-fachen Säurekonzentration im Vergleich zu pH 6.
- Zitronensaft und Essig besitzen pH-Werte von etwa 2.4-2.5.
Säuremantel der Haut
Während Blut mit pH-Wert 7,4 eine schwach basische Reaktion zeigt, ist der Hydrolipidfilm der Hautoberfläche mit pH-Werten von 4,5 bis 5,5 je nach Person und Körperregion leicht sauer. Der niedrige Haut-pH-Wert resultiert aus dem oxidativen Abbau von Hautbarriere-Bestandteilen durch die Hautflora. Dabei werden Säuren gebildet. Der so aufgebaute "Säuremantel" hilft, insbesondere auch den lokal adaptierten, residenten Keimpopulationen, fremde, von außen kommende Mikroorganismen weitgehend fernzuhalten. Aus diesem Blickwinkel ist der unkritische Einsatz starker Antioxidantien in Hautpflegemitteln möglicherweise kontraproduktiv, da er die oxidative Tätigkeit des Hautmikrobioms mitbeeinflusst. Im Übrigen ist der pH-Wert bei Barrierestörungen wie atopischer Haut und irritativen Kontaktdermatosen erhöht.
Pufferwirkung der Haut
Säuren können mit Basen neutralisiert werden. Bei fortschreitender Neutralisation von Säuren mit Basen steigt der pH kontinuierlich an, bis pH 7 erreicht ist. Zum Beispiel entsteht aus Salzsäure und Natronlauge das aus der Küche bekannte Kochsalz (Natriumchlorid). Wässrige Lösungen von Kochsalz verhalten sich "pH-neutral".
Die Hautoberfläche kommt tagtäglich mit unterschiedlich sauren und basischen Stoffe zusammen. Sie würden den Haut-pH-Wert laufend verändern und dadurch physiologische, meist enzymatische Vorgänge stören, die einen bestimmten pH benötigen. Genau dies wird jedoch durch die spezielle Zusammensetzung der Hautoberfläche verhindert; sie hält den Haut-pH trotz der Einwirkung fremder Stoffe bis zu einem gewissen Grad konstant. Zusammensetzungen dieser Art bezeichnet man allgemein als "Puffer". Die damit verbundene Pufferkapazität der Haut, also in welcher Größenordnung äußere Einflüsse kompensiert werden können, ist zwar nicht sehr groß, aber völlig ausreichend, dass zum Beispiel Pflegecremes mit pH < 7 und Wasser mit pH 7 den Haut-pH nicht verändern. Mit anderen Worten: Es macht keinen Unterschied, ob eine Creme mit pH 6,5 oder pH 5 appliziert wird; sie muss also nicht unbedingt "pH-hautneutral" (pH 5,5) sein.
Hautirritationen
Ganz anders ist die Situation, wenn ein Präparat oder eine Chemikalie auf die Haut gelangt, die selbst eine hohe Pufferkapazität besitzt. Das ist häufig bei Arbeitsstoffen der Fall. Dann reicht beispielsweise bereits ein länger anhaltender Kontakt mit einem Medium von pH 8, dass die Haut stark angegriffen wird. Gleiches gilt für Werte, die unter pH 4 liegen wie etwa bei konzentrierten Fruchtsäuren, die auf diese Weise keratolytisch wirken (Fruchtsäure-Peeling). So kommen Verätzungen vor, wenn die empfohlenen Behandlungszeiten überschritten werden. Die gleiche Peeling-Wirkung wäre selbstverständlich auch mit verdünnter Salzsäure zu erreichen, nur lässt sich diese aufgrund ihres Namens weniger gut vermarkten.
Mit diesen gezielten Irritationen sind nachfolgend Regenerationsleistungen der Haut verbunden. Was einmalig aufgrund dermatologischer Indikationen und kosmetischer Konditionen Sinn macht, ist bei routinemäßigen und über längere Zeit erfolgenden Behandlungen mit Langzeit-Nebenwirkungen wie Rosacea und perioraler Dermatitis verbunden. D. h. die Haut reagiert wie bei Strahlenschäden kumulativ – sie vergisst nichts.
Nicht nur Flüssigkeiten, sondern auch feste Stoffe können bei längerem Kontakt den Säuremantel zerstören. Ein typisches Beispiel ist das als Füllstoff in Kartonagen eingesetzte Calciumcarbonat. Es reagiert mit den hauteigenen Fettsäuren unter Bildung von Calciumseifen, während die Kartonagen als solche zusätzlich entfettend wirken. Wenn beim täglichen Arbeiten mit Kartonagen nicht konsequent ein Hautschutz oder Handschuhe verwendet werden, sind Dermatosen die Folge. Die Gefährdung der Haut durch Kalk und Zement bei Tätigkeiten auf dem Bau ist noch weitaus größer.
Altershaut
Im Vergleich zu jugendlicher Haut besitzt die Altershaut statistisch einen höheren Wert von pH 6. Mit entsprechenden, auf z. B. pH 4,5 gepufferten Präparaten wird versucht, den Haut-pH dauerhaft nach unten zu korrigieren. Der dahinter stehende Gedanke ist es, den Stoffwechsel der Haut, der durch Enzyme gesteuert wird, optimal zu erhalten. Inwieweit diese Strategie tatsächlich Erfolg hat, hängt von einigen offenen Fragen ab:
- Ist die pH-Erhöhung der Hautoberfläche kulturbedingt oder eine eher pathologische Alterserscheinung?
- Sind auch in tieferen Hautschichten mit ihren Stoffwechselleistungen altersbedingte pH-Veränderungen festzustellen?
- Inwieweit hat der pH der Hautoberfläche einen Einfluss auf Bereiche, in denen Enzyme tätig sind?
- Welche Rolle spielt das Mikrobiom beim pH der Altershaut?
Zur Ermittlung der tatsächlichen Kausalitäten sind noch umfangreiche Studien notwendig.
Kosmetische Präparate
Kosmetika werden in der Regel mit teilneutralisierten Salzen der Phosphor- und Zitronensäure oder Mischungen derselben gepuffert. INCI: Disodium Phosphate, Potassium Phosphate, Disodium Citrate etc. Zuweilen werden diese Salze auch direkt bei der Herstellung der Kosmetika gebildet. Dann findet man auf der Zutatenliste z. B. Citric Acid (Zitronensäure) und die Neutralisationsmittel (Basen): Sodium Hydroxide (Natriumhydroxid), Potassium Hydroxide (Kaliumhydroxid). Selbstverständlich sind dann Letztere, bei denen es sich um Gefahrstoffe handelt, nicht mehr im Endprodukt enthalten.
Konventionelle Stückseifen bestehen aus Fettsäuresalzen, im einfachsten Fall aus Natriumstearat oder Natriumpalmitat (Kernseife). Sie verursachen beim Waschen einen pH von weit über 7, weil es sich um Salze einer starken Base mit einer schwachen Säure handelt. Der hohe pH ist für die Haut nicht förderlich. Daher wurden Kernseifen von den pH-neutralen und schwach sauren Flüssigseifen abgelöst. In Leitungswässern mit hoher permanenter und temporärer Härte können geringe (!) Mengen Kernseife (kurzes Eintauchen) aber hilfreich sein, das Wasser zu enthärten und die Oberflächenspannung zu senken. Die dabei ausflockenden Kalkseifen sind zwar eine unschöne Begleiterscheinung, das Wasser ist dann aber sehr gut für barrieregestörte Haut geeignet, da die Härtebildner die Barriere nicht mehr weiter schädigen können.
Viele der im Anhang der Kosmetikverordnung stehenden Konservierungsstoffe haben ihr Wirkungsoptimum im leicht sauren pH-Bereich. Dies gilt naturgemäß vor allem für die dort gelisteten Säuren. In diesem Zusammenhang ist interessant, dass es Wirkstoffe gibt, die bei niedrigen pH-Werten eine höhere Oxidationsstabilität besitzen. Dies trifft z. B. auf den Hauptwirkstoff des grünen Tees, das Epigallocatechingallat (EGCG), zu. EGCG ist ein Polyphenol, das sich unter anderem bei Teeaufgüssen rasch dunkel verfärbt. EGCG stimuliert die Bildung von Filaggrinen und wirkt Kollagenase-hemmend. Mit Fumarsäure oder Zitronensäure bleibt es hell und stabil.
Dr. Hans Lautenschläger | 
