Zunächst ging es um den Hautschutz und die Behandlung trockener Hautzustände. Danach um die gezielte Befeuchtung der Haut, bis die Bedeutung der Barrierelipide der Haut erkannt wurde. Mit dem Bestreben, kranke Hautzustände wie atopische Dermatitis (AD) und Psoriasis zu behandeln, wuchsen auch die Erkenntnisse über die biochemischen Abläufe in der Haut, die Rolle der Gene und die Besiedlung der Haut mit Mikroorganismen. Seit dem letzten Jahrzehnt häufen sich Hinweise, dass nicht nur das Mikrobiom der Haut, sondern das humane Mikrobiom insgesamt eine Schlüsselrolle auch bei der Hautgesundheit spielt. Von Petrolatum zum NMF Ich verorte den Startpunkt moderner Kosmetik im Jahr 1872, in dem Robert Cheseborough begann, das Mineralölderivat Petrolatum als Vaseline zu vermarkten (1). Vaseline ist sozusagen der Prototyp eines Hautschutzmittels, dessen Wirksamkeit darin besteht, einen Schutzfilm über die Haut zu legen, um so die Barrierefunktion zu verbessern und das Eindringen von Wasser (und wasserbasierten Schadstoffen) zu verhindern. Zudem wurde es im Gegensatz zu den damals alternativ verwendeten tierischen Fetten nicht ranzig, und konnte für (fast) alles verwendet werden. Zu jener Zeit wurden auch pharmazeutische Rezepturen entwickelt, die die damals gängigen Inhaltsstoffe wie Lanolin, Vaseline und Paraffinöl enthielten. Sie finden sich heute noch in den Pharmakopöen z.B. als Eucerinum anhydricum (Wollwachsalkoholsalbe, Magistralrezeptur). Während der Beitrag die Lipid-Komponenten der Haut zur Hautbefeuchtung lange kontrovers diskutiert wurde, sah die Sache für Wasser und andere Befeuchtungsmittel anders aus. 1952 veröffentlichte Blank erste Untersuchungen, wie Haut befeuchtet werden kann, und identifizierte Wasser als den wichtigsten Faktor für die Elastizität der Haut. 1959 beschrieb Jacobi die Zusammensetzung des Natural Moisturizing Factors (NMF) (3). Die Haupteigenschaft der NMF-Komponenten ist ihre Hygroskopizität, die somit auch als relevant postuliert wurde, um in vivo gegen Austrocknung der Haut zu schützen. 1984 entwickelte Takahashi (4) eine Methode, um die mechanischen Eigenschaften von isoliertem Stratum Corneum (SC) zu beurteilen. Die Arbeitsgruppe untersuchte die Effekte von Wasser, Glycerin und den NMF-Komponenten. Dabei konnten sie die Elastizitätssteigerung der behandelten Haut mit der Wasserbindekapazität der Haut korrelieren. Jahre später wurde dann entdeckt, dass die NMF-Komponenten Abbauprodukte des Filaggrins (5) sind und die Abwesenheit bestimmter NMF-Komponenten also kein Auslöser, sondern Ergebnis bestimmter krankhafter Hautzustände ist. Heute, mit genanalytischen Methoden (6), sieht man die NMF-Komponenten als Biomarker bestimmter Filaggrin-Genotypen an (7). Damals wurde auch Glycerin untersucht, das erwiesenermaßen eine gute in vivo Hautbefeuchtungsleistung hat, in den in vitro Experimenten aber schlecht abschnitt. Sein Wirkmechanismus beruht auf der Stimulation der Expression von Aquaporin-3. Agre identifizierte 1990 Aquaporine als Strukturen, die in allen Membranen vorkommen. Generell dienen Hautbefeuchtungsmittel zum Erhalt der Elastizität der Haut (Schutz vor mechanischen Einwirkungen), zur Schaffung idealer Bedingungen für hydrolytische Enzyme (ordentliche Funktion der Desquamation = Abschuppung der oberen Hautzellen) und zur Stimulation der Aquaporin-3 Expression in Keratinocyten (Beitrag zur Barrierefunktion). Während erste Wirksamkeitsuntersuchungen damals gerne an isoliertem SC gemacht wurden, gilt heute die in vivo Messung als „Gold-Standard". Etablierte Methoden zur Messung des Hautzustandes in vivo sind Hautbefeuchtung (elektrische Kapazität), Trockenheit bzw. Barrierefunktion (TEWL) und Hautrauigkeit. Die Lipidbarriere und die Haut: Ceramide und Fettsäuren In den 1950er Jahren wurde zunehmend die Struktur der Haut untersucht (10) und ihre Lipidzusammensetzung analysiert (11, 12). Der Wendepunkt im Verständnis begann 1975 mit der Publikation von Elias und Friend (13). Sie verwenden ein Elektronenmikroskop und beschreiben extensiv die Präparations- (Gefrierbruch und Fixierung mit RuO4 und OsO4) sowie die Analysemethoden für Hautbiopsien. Im Stratum Granulosum identifizierten sie „lamellare Granulen" und vermuteten lipidreiche Regionen im SC. In der Folge dieser Entdeckungen wurden Hunderte weiterer Untersuchungen unternommen und die lipidreichen Regionen bestätigt. Als die Lipide im SC wurden drei Hautgruppen identifiziert, die in einem molaren Verhältnis von 1:1:1 vorliegen: Ceramide, Cholesterin und freie Fettsäuren. 1988 veröffentlichte Elias das „Ziegelstein-Mörtel-Modell" des SC (14). Kernpunkt des Models ist der Mörtel, strukturierte Lipid-Doppelschichten. Diese sollten für eine intakte Barriere der Haut verantwortlich sein. Mit der Korrelation verschiedener analytischer Methoden wie Hautbiopsien, die Analyse der jeweiligen Zusammensetzung der epidermalen Lipide, Elektronenmikroskopie, Röntgenbeugung, visuellen Beurteilungen, in vivo TEWL Messungen, konnten Struktur-Wirkungs-Beziehungen belegt werden. Im Zuge solcher Untersuchungen wurden auch neun Ceramide in menschlicher Haut isoliert. Ceramide spielen eine essentielle Rolle in der Bildung der Lipid-Doppelschichten des SC. Ihre Abwesenheit kann klar mit kranken Hautzuständen korreliert werden (15-18). Abbildung: Nomenklatur der Ceramide Bei der Stratifizierung der Epidermis finden molekulare und enzymatische Veränderungen der Lipide statt (19-21). Die Vorläufer der Barrierelipide werden dabei zunächst im Golgiapparat der lebenden Zelle gebildet und dann in den Lamellaren Granulen umgewandelt. Dort werden die Lipide zusammen mit einer großen Menge unterschiedlicher Enzyme ausgeschieden, oder zum Teil schon in situ abgebaut. 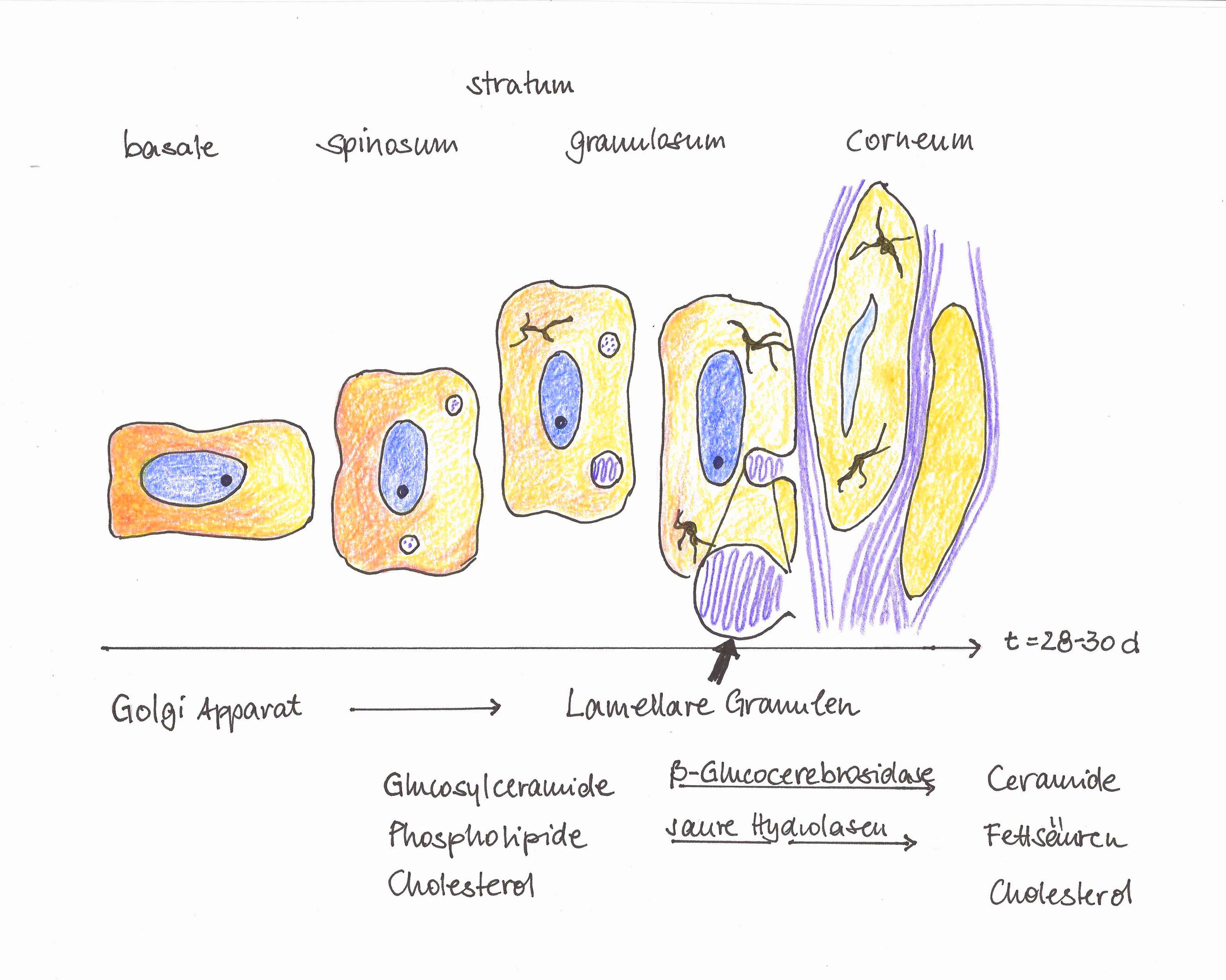
Abbildung: Differenzierung der Epidermis und Ausscheidung von Lipiden Nimmt man alle diese Ergebnisse zusammen, wären Ceramide eigentlich die Top-Kandidaten zur Therapie erkrankter Haut: eine topische Supplementierung dieser Substanzen sollte eine effektive Therapie für Psoriasis und Atopische Dermatitis (AD) sein und einer Kortison-Behandlung deutlich vorzuziehen. Allerdings zeigen sich Ceramide bei der Anwendung allein dem Steroid nicht überlegen (22). Dennoch werden Ceramide in der Kosmetik als effektive Hautpflegesubstanzen eingesetzt. Doch in der Lipidbarriere befindet sich noch eine Substanzgruppe, die es wert ist, genauer betrachtet zu werden - Fettsäuren. Da die Epidermis ein stoffwechselaktiver Ort für die Lipidsynthese ist, werden die meisten Fettsäuren von den Keratinozyen de novo synthetisiert. Dabei ist das Stratum Granulosum der aktivste Bereich (23).
Fettsäuren spielen eine Schlüsselrolle bei der (Haut)-Gesundheit. Besonders sind dieses essentielle Fettsäuren (EFA), welche nicht durch den Körper selber synthetisiert werden können und mit der Nahrung zugeführt werden müssen. Sie regulieren Membranfunktionen, den Cholesterinmetabolismus, wirken als aktive ß-Blocker, Diuretika, sowie anti-hypertensiv und anti-arteriosklerotisch (24). Darüber hinaus ist Linolsäure die Acylkomponente von Ceramid-1; die Therapie von AD mit Nachtkerzenöl (reich an γ-Linolensäure) ist besonders bei Kindern erfolgreich. Entzündungen der Haut bei Atopischer Dermatitis (AD) und Psoriasis Entzündliche Erkrankungen der Haut wie AD und Psoriasis sind von großer gesellschaftlicher Relevanz. Sie betreffen überwiegend Menschen in der westlichen Welt mit einer Prävalenz bei der erwachsenen Bevölkerung von 3% bzw. 2%. Darüber hinaus ist AD während des letzten Jahrhunderts über das 2- bis 3-fache angestiegen. Eine wirksame Behandlung würde die Lebensqualität vieler Menschen erhöhen. Bisher lässt sich allenfalls der Juckreiz, der häufig mit AD einher geht, mit Kortison lindern; nach neueren Studien sind jetzt auch Antikörper entwickelt wurden, die Juckreiz mindern (26). Die mangelnde Effektivität der Behandlungsmethoden liegt u.a. daran, dass nicht geklärt ist, welche Mechanismen diese Krankheiten auslösen. Darüber hinaus scheinen die Störungen der Hautbarriere nur eines von vielen Symptomen zu sein, die ihrerseits das System wieder beeinflussen. Heute ist bekannt, dass nicht nur die Barrierelipide in das Geschehen bei AD involviert sind, neben Entzündungsmediatoren (27) - in ekzematischer Haut lassen sich erhöhte Level von Prostaglandin E2 und Leukotrien B4 und erniedrigte von Interleukin-1α nachweisen - sind auch das Immunsystem modulierende Stoffe beteiligt. Diese werden sowohl von innen wie auch von außen getriggert. Psoriasis und AD sind insofern ähnlich, als dass sie komplexe, ererbte Erkrankungen sind, die Gene involvieren, die die Immunkomponenten und Strukturproteine kodieren, die die Differenzierung der epidermalen Zellen regulieren (28, 29). Es mehren sich Hinweise, dass diese Erkrankungen gehäuft mit anderen Krankheiten zusammen vorkommen. AD mit Asthma, Allergien und Psoriasis mit metabolischen Krankheiten (Diabetes), Arteriosklerose, Rheumatische Arthritis sowie psychologischen Störungen. Es wird mittlerweile diskutiert, ob diese (Stoffwechsel-)Erkrankungen die Ursache sind und die Läsionen der Haut eine Art Frühwarnsystem, das dem Ausbruch vorausgeht (28). Während es ein effektives Therapeutikum für Psoriasis gibt wie Cyclosporin A, gibt es keinerlei für AD. Zusätzlich führt bei der AD eine Kolonisation der Haut mit pathogenen Keimen wie Staphylococcus aureus zu weiteren Komplikationen. Das Biotop der Haut und mögliche zukünftige Forschungsfelder Neuere Untersuchungen, die unter dem Stichwort „Humanes Mikrobiom" veröffentlicht worden sind, zeigen, dass die menschlichen Körper als riesiges Habitat für Mikroorganismen aller Art dienen (31). Epidemiologische Untersuchungen des Darmmikrobioms deuten darauf hin, dass dort die genetische und metabolische Diversität des Menschen am größten ist. Der Vergleich von Stuhlproben von Personen aus ländlichen Gegenden der Dritten Welt mit denen von Personen aus urbanen Regionen der USA, zeigten signifikante Unterschiede in der phylogenetischen Zusammensetzung der Stuhlmikroben. Die aus den USA war die am wenigsten diverse (34). Es ist unser Lebensstil, besonders die Ernährungsgewohnheiten, die einen signifikanten Einfluss auf das Darmmikrobiom haben und somit gesundheitsrelevant sind. Es wird vermutet, dass die höhere Inzidenz von Allergien, Asthma und einigen Autoimmun-Erkrankungen in der westlichen Welt mit der Zusammensetzung des Darmmikrobioms zusammenhängt (35, 36). Das Mikrobiom der Haut ist nicht so divers wie das des Darms, aber auch hier bedecken eine Vielzahl von Mikroorganismen (Viren, Bakterien und Pilze) und Milben die Oberfläche und „wohnen" tief in den Haarschäften und Drüsen. Exogene und endogene Faktoren beeinflussen die Besiedelung der Haut wie:
- Physiologie des Wirtes: Geschlecht, Alter, Lokalisation
- Genotyp des Wirtes: Störanfällige Gene wie Filaggrin
- Umgebung: Klima, geographischer Ort
- Lifestyle: Beruf, Hygiene
- Immunsystem: frühere Exposition, Entzündung
- Pathobiologie: Zugrunde liegende Ursachen wie z.B. Diabetes
Insgesamt ist unsere Haut mit mehr als 1 Milliarde Bakterien / cm2 besiedelt, welche eine fundamentale Rolle in der Hautphysiologie spielen. Staph. epidermidis ist eines der dominanten Bakterien auf unserer Haut und produziert nicht nur AMPs, sondern sondert auch Proteasen ab, die die Ausbildung von Biofilmen durch pathogene Spezies beschränken (37). Dabei ist lässt sich das Verhältnis von Staph. aureus / Staph. epidermidis mit der Schwere der AD korrelieren (22, 32, 38). Nimmt man die derzeitigen Ergebnisse zusammen, deutet alles darauf hin, dass AD eine erworbene Erkrankung ist. Es steht zu erwarten, dass zukünftige Untersuchungen sich mehr auf die individuelle mikrobielle Besiedlung der Patienten konzentrieren werden. Da das Mikrobiom der Haut aber auch die erste Barriere unserer Haut ist, werden wir vermutlich auch unsere Reinigungs- und Pflegegewohnheiten kritisch hinterfragen. Speziell die Verwendung von Konservierungsmitteln in Kosmetikprodukten. Da aber auch das Darmmikrobiom einen relevanten Beitrag zu unserem Immunsystem leistet, werden wir in Zukunft stärker darauf achten, was wir essen. Aber eigentlich ist das ja nicht neu: Wir wissen, dass gesunde, schöne Haut von Innen kommt. Literatur - David S Morrison, Petrolatum: a useful classic, Cosmet Toil (1996) 111:59-69
- http://www.gpo.gov/fdsys/pkg/CFR-2012-title21-vol5/pdf/CFR-2012-title21-vol5-part347.pdf
- Irvin H Blank, Factors which influence the water content of the stratum corneum, J Invest Dermatol (1952) 18: 433-440
- Motoji Takahashi, Masami Yamada, Yashuhiko Machida, Yukiko Tsuda, A new method to evaluate the softening effect of cosmetic ingredients on skin, J Soc Cosmet Chem (1984) 35: 171-181
- Anthony V Rawlings, Ian R Scott, Clive R Harding, Paul Bowser, Stratum corneum moisturization at the Molecular Level, J Invest Dermatol (1994) 103: 731-740
- Joseph Fowler, Understanding the role of natural moisturizing factor in skin hydration, Practical Dermatol (6/2012):36-40
- S Kezic, A Kammeyer, F Calkoen, JW Ruhr, JD Bos, Natural moistruzing factor components in the stratum corneum as biomarkers of filaggrin genotype: evaluation of minimal invasive methods, BJD (2009) 161: 1098-1104
- Clive R Harding, John Bartolone, Anthony V Rawlings, Effects of natural moisturizing factor and lactic acid isomers on skin, Dry Skin and Moisturizers: Chemistry and Function, Marie Loden, Howard I. Maibach, Eds (CRC Press) (2000): 229-241
- Ghita Lanzendörfer, Lipidic ingredients in skin care formulations, Cosmetic Lipids and the Skin Barrier, Thomas Förster Ed (Marcel Dekker) (2002): 255-297
- Albert M Kligman, A brief history of how the dead stratum corneum became alive, Skin Barrier, Elias, Feingold Eds. (CRC Press) (2006): 15-24
- Apostolos Pappas, Epidermal surface lipids, Dermato-Endocrin (2009) 1:2: 72-76
- ME Stewart, DT Downing, PE Pochi, JS Strauss; The fatty acids of human sebaceous gland phosphatidylcholin, Biochim Biophys Acta (1978), 529: 380-386
- Peter M Elias and Daniel S Friend: The permeability barrier in mammalian epidermis, J Cell Biol (1975) 65: 180-191
- Peter M Elias, Structure and function of the stratum corneum permeability barrier, Drug Dev Res (1988) 13: 97-105
- Volker Schreiner, Gert S Gooris, Stephan Pfeiffer, Ghita Lanzendörfer, Horst Wenck, Walter Diembeck, Ehrhardt Proksch, Joke Bouwstra, Barrier characteristics of different human skin types Investigated with X-ray diffraction, lipid analysis, and electron microscopy imaging, J Invest Dermatol (2000) 114: 654-660
- PM Elias, GK Menon, Structural and lipid biochemical correlates of the epidermal lipid barrier, Adv Lipid Res (1991) 24: 1-26
- M Fartasch, Epidermal barrier disorders in skin, Microsc Res Tech (1997) 38: 361-372
- G Imokawa, A Abe, K Jin, M Kawashima, A Hidano, Decreased level of ceramides in stratum corneum of atopic dermatitis: an etiologic factor in atopic dry skin? J Invest Dermatol (1991) 90: 523-526
- Marilyn A Lampe, Mary L Williams, Peter M Elias, Human epidermal lipids: characterization and modulations during differentiation, J Lipid Res (1983) 24:131-140
- Philip W Wertz, Lipids and barrier function of the skin, Acta Derm Venerol (2000) 208: 7-11
- Kathi C Madison, Barrier function of the skin: "la raison d'ètre" of the epidermis, J Invest Dermatol (2003) 121: 231-241
- Peter M Elias, Skin barrier function, Curr Allergy Asthma Rep (2008) 8: 299-305
- Denis Khnykin, Jeffrey H Miner, Frode Jahnsen, Role of fatty acid transporters in epidermis - implications for health and disease, Dermato-Endocrin (2011) 3:2: 53-61
- Undurti N Das, Essential fatty acids: biochemistry, physiology, pathology, Biotechnol J (2006) 1: 420-439
- M-T Huang, G Ghai, C-T Ho, Inflammatory process and molecular targets for antiinflammatory nutraceuticals, Comp Rev Food Sci Food Safety (2004) 3: 127-139
- Nemoto, M Furure, H Nakagawa, M Shiramoto, R Hanada, S Matsuki, S Imayama, M Kato, I Hasebe, K Taira, M Yamamoto, R Mihara, K Kabashima, T Rusicka, J Hanifin Y Kumagai, The first trial of CIM331, a humanized antihuman interleukin-31 receptor A antibody, in healthy volunteers and patients with atopic dermatitis to evaluate safety, tolerability and pharmacokinetics of a single dose in a randomized, double-blind, placebo-controlled study, BJD (2015) 14: 76-82
- DM Reilly, R Parslew, GR Sharpe, B Powell, MR Green, Inflammatory mediators in normal, sensitive and diseased skin types, Acta Derm Venerol (2000) 80: 171-174
- Emma Guttman-Yassky, Kristine E Nograles, James G Krueger, Constrasting pahtogenesis of atopic dermatitis and psoriasis - Part I: clinical and pathologic concepts, J Allergy Clin Immunol (2011) 127: 1110-1118
K Reich, The concept of psoriasis as a systemic inflammation: implications for disease management, Journal of the European Academy of Dermatology and Venereology (2012) 3-11
M Boguniewicz, DV Leung, Atopic dermatitis: a disease of altered skin barrier and immune dysregulation, Immonol Rev (2011); 242: 233-246 - Emma Guttman-Yassky, Kristine E Nograles, James G Krueger, Constrasting pahtogenesis of atopic dermatitis and psoriasis - Part II: Immune cell subset and therapeutic concepts, J Allergy Clin Immunol (2011) 127: 1420-1432
- Nikhil Dhingra, Emma Guttman-Yassky, A possible role for IL-17A in establishing Th2 inflammation in murine models of atopic dermatitis, J Invest Dermatol (2014) 134:2071-2074
RL Gallo, T Nakatsuji, Microbial symbiosis with the innate immune defense system of the skin, J Invest Dermatol (2011) 131: 1974-1980
Jürgen Schauber, Richard L Gallo, Antimicrobial peptides and the skin immune defense system, J Allergy Clin Immunol. (2008) 122: 261-266
Guangshun Wang, Human Antimicrobial Peptides and Proteins, Pharmaceuticals (2014) 7: 545-594 - The Human Microbiome Project Consortium, Structure, function and diversity of the healthy human microbiome, Nature (2012) 486: 207-214
- Elizabeth A Grice, Julia A Segre, The skin microbiome, Nat Rev Microbiol (2011) 9: 244-153
- Elizabeth A Grice, Heidi H Kong, Sean Conlan, Clayton B Deming, Joie Davis, Alice C Young, NISC Comparative Sequencing Program, Gerard G Bouffard, Robert W Blakesley, Patrick R Murray, Eric D Green, Maria L Turner, Julia A Segre, Topographical and temporal diversity of the human skin microbiome, Science (2009) 324: 1190-1192
- Tanya Yatsunenko, Frederico E Rey, Mark J Manary, Indi Trehan, Maria Gloria Dominguez-Bello, Monica Contreras, Magda Magris, Gilda Hidalgo, Robert N Baldassano, Andrey P Anokhin, Andrew C Heath, Barbara Warner, Jens Reeder, Justin Kuczynski, J Gregory Caporaso, Catherine A Lozupone, Christian Lauber, Jose Carlos Clemente, Dan Knights, Rob Knight, Jeffrey I Gotdon, Human gut microbiome viewed actross age and geography, Nature (2012) 486: 222-228
- Alison N Thorburn, Laurence Macia, Charles R Mckay, Diet, metabolites and "western-lifestyle" inflammatory diseases, Immunity (2014) 40: 833-842
- Pieter C Dorrestein, Sarkis K Mazmanian, Rob Knight, Finding the missing links among metabolites, microbes and the host, Immunity (2014) 40: 824-832
- RL Gallo, T Nakatsuji, Microbial symbiosis with the innate immune defense system of the skin, J Invest Dermatol (2011) 131: 1974-1980
- Yasmin Bekkair, Shruti Naik, compartmentalized ad systemic control of tissue immunity by commensals, Nature Immunology (2013) 14: 646-65
Dr. Ghita Lanzendörfer-Yu Langfassung:
Ghita Lanzendörfer-Yu, Skin Structure and Requirements on Skin Care - From Past to Future, Lecture on 4th International Symposium on Corneotherapy, May 6-8, 2016, Cologne, Proceedings 12-24
|

